 Arsenik och kadmium är två grundämnen som är giftiga för människan och som förekommer naturligt i berggrunden. Arsenik kan förgifta grundvatten, vilket leder till att lokalbefolkningen på vissa ställen i världen ständigt utsätts för giftet.
Arsenik och kadmium är två grundämnen som är giftiga för människan och som förekommer naturligt i berggrunden. Arsenik kan förgifta grundvatten, vilket leder till att lokalbefolkningen på vissa ställen i världen ständigt utsätts för giftet.
– Vissa grödor, särskilt ris, tar upp arsenik mycket effektivt eftersom proteinerna på rötterna inte kan skilja på arsenik och det livsnödvändiga grundämnet fosfor, säger Therese Jacobson, doktorand vid institutionen för kemi och molekylärbiologi. Kadmium sprids i sin tur främst genom bland annat konstgödning och cigarettrök.
Hennes doktorsavhandling handlar om forskning för att förstå hur celler reagerar på och försvarar sig mot arsenik och kadmium. Therese Jacobson och hennes kollegor har lyckats identifiera en försvarsmekanism hos jästceller. Mekanismen utsöndrar en viss sorts molekyl, glutation, som består av tre aminosyror och som binder till arsenik utanför cellerna.
– Genom bindningen hindras arseniken från att tas upp i cellerna, säger Therese Jacobson.
Bidrar till att proteiner klumpar ihop sig
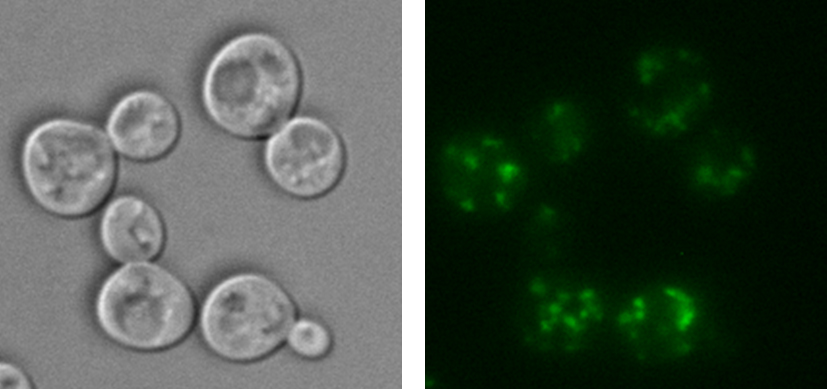
 Therese Jacobson har i sin forskning även konstaterat att arsenik och kadmium bidrar till att proteiner klumpar ihop sig och bildar så kallade aggregat. Sådan aggregering är i sin tur negativ för cellerna – flera neurodegenerativa sjukdomar, som Alzheimers och Parkinsons, är kopplade till att protein bildar aggregat. Therese Jacobsons forskning visar att arsenik och kadmium bidrar till proteinaggregering på olika sätt.
Therese Jacobson har i sin forskning även konstaterat att arsenik och kadmium bidrar till att proteiner klumpar ihop sig och bildar så kallade aggregat. Sådan aggregering är i sin tur negativ för cellerna – flera neurodegenerativa sjukdomar, som Alzheimers och Parkinsons, är kopplade till att protein bildar aggregat. Therese Jacobsons forskning visar att arsenik och kadmium bidrar till proteinaggregering på olika sätt.
– Arsenik förhindrar funktionaliteten hos hjälpproteinen chaperoner, säger Therese Jacobson. Chaperoner har till uppgift att hjälpa nybildade proteiner att anta sin rätta tredimensionella form. Om de nybildade proteinerna inte antar sin rätta form så ökar sannolikheten för att de klumpar ihop sig med andra proteiner och bildar aggregat.
Kadmium påverkar i sin tur zink-bindande proteiner. Zinkjoner är viktiga för att vissa proteiner ska anta sin rätta form, och forskningen visar att kadmium tycks ersätta zink i de här proteinerna och därmed leda till aggregering.
Kontakt
Therese Jacobson, doktorand, institutionen för kemi och molekylärbiologi
therese.jacobson@gu.se, 031-786 2588, 0736-381060
Länk till avhandlingen
Cellular Responses to Arsenite and Cadmium - Mechanisms of Toxicity and Defense in Saccharomyces cerevisiae
 Arsenik och kadmium är två grundämnen som är giftiga för människan och som förekommer naturligt i berggrunden. Arsenik kan förgifta grundvatten, vilket leder till att lokalbefolkningen på vissa ställen i världen ständigt utsätts för giftet.
Arsenik och kadmium är två grundämnen som är giftiga för människan och som förekommer naturligt i berggrunden. Arsenik kan förgifta grundvatten, vilket leder till att lokalbefolkningen på vissa ställen i världen ständigt utsätts för giftet. Therese Jacobson har i sin forskning även konstaterat att arsenik och kadmium bidrar till att proteiner klumpar ihop sig och bildar så kallade aggregat. Sådan aggregering är i sin tur negativ för cellerna – flera neurodegenerativa sjukdomar, som Alzheimers och Parkinsons, är kopplade till att protein bildar aggregat. Therese Jacobsons forskning visar att arsenik och kadmium bidrar till proteinaggregering på olika sätt.
Therese Jacobson har i sin forskning även konstaterat att arsenik och kadmium bidrar till att proteiner klumpar ihop sig och bildar så kallade aggregat. Sådan aggregering är i sin tur negativ för cellerna – flera neurodegenerativa sjukdomar, som Alzheimers och Parkinsons, är kopplade till att protein bildar aggregat. Therese Jacobsons forskning visar att arsenik och kadmium bidrar till proteinaggregering på olika sätt.