- Hem
- Forskning
- Hitta forskning
- Junchi Huang - Osteoclasts in the fight against metastatic prostate cancer
Junchi Huang - Osteoclasts in the fight against metastatic prostate cancer
Junchi Huang disputerade den 14 december på en avhandling för medicine doktorsexamen vid Sahlgrenska akademin, institutionen för kliniska vetenskaper, inom ämnet urologi
Titel på avhandlingen: The roles of osteoclasts and RUNX2 in the progression of prostate cancer bone metastases

En kort sammanfattning på engelska
Den svenska sammanfattningen
Prostatacancer är en av de cancerformer som orsakar flest dödsfall bland män i Sverige. Det är oftast inte tumören i prostata som orsakar lidande och död, utan cancer som spridit sig till andra organ i kroppen och bildat dottertumörer, metastaser. Om cancern hittas tidigt, innan den hunnit sprida sig kan man i många fall behandla och bota sjukdomen. Metastaserad cancer går idag inte att bota, även om det finns många läkemedel som förlänger livet betydligt.
Skelettet är det vanligaste organet för metastaser från prostatacancer. Om man upptäcker metastaser från prostatacancer behandlas patienten oftast med så kallad hormonbehandling, vilken stoppar produktionen av det manliga könshormonet steroiden testosteron och hindrar därmed cancercellerna från att växa ytterligare. Denna behandling har god effekt hos de flesta, men tyvärr brukar sjukdomen ta fart igen efter några år. Den har då blivit kastrationsresistent, d.v.s. den växer trots att halterna av testosteron i blodet fortfarande är låga.
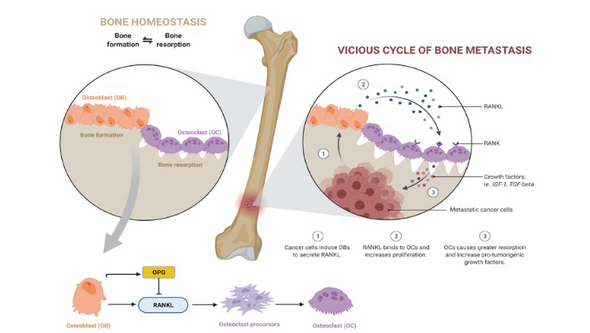
I skelettet växer tumören i benmärgen och metastaser från prostatacancer leder oftast till att ben-nybildningen ökar, i motsats till flera andra cancerformer, som bröstcancer och lungcancer, vilka oftast leder till en ökad nedbrytning av benet. Cancercellerna samverkar med olika typer av celler som finns i benet och benmärgen, och det är känt sedan tidigare att nedbrytning av benvävnad frigör flera substanser som kan driva på cancercellernas tillväxt. I tidigare studier har vi studerat hur osteoblaster, dvs de celler som bygger benvävnad, interagerar med prostatacancerceller och funnit att de påverkar cancercellerna så att de förbättrar sin förmåga att själva bilda testosteron och stimulera sin tillväxt.
Osteoklaster är de celler som bryter ner benvävnad och som i ett friskt ben samverkar med osteoblaster för att ständigt förnya och behålla benvävnaden i gott skick. Om och på vilket sätt osteoklaster direkt kan påverka prostatacancercellernas egenskaper har tidigare inte varit känt.
I denna avhandlings första delarbete odlas prostatacancerceller tillsammans med osteoklaster och effekterna av detta studeras. Osteoklaster påverkar cancercellerna till att dela sig fortare och dö mer sällan. Uttrycket av ca 3500 gener förändrades i cancercellerna efter samodling med osteoklaster. Generellt påverkades prostatacancerceller som ger upphov till ben-nedbrytande metastaser mer än de prostatacancerceller som ger upphov till benbildande metastaser. Gener som medverkar till att DNA kan repareras uppreglerades av osteoklaster främst i de ben-nedbrytande prostatacancercellerna. En grupp gener som reglerar hur cellerna påverkas av en viss storts stress påverkades i båda cancercelltyperna.
RUNX2 är ett protein som i normala fall styr hur osteoblaster bildas. Det är sedan tidigare känt att RUNX2 också finns i prostatacancerceller och gör dessa mer elakartade. Vi har i tidigare studier sett att osteoblaster ökar mängden RUNX2 i benbildande prostatacancerceller.
I avhandlingens andra delarbete studerar vi hur osteoklaster påverkar RUNX2 i prostatacancerceller och hur RUNX2 reglerar förekomst av vissa enzymer som medverkar i steroidsyntesen och bildningen av testosteron. På samma sätt som osteoblaster, ökar osteoklaster mängden RUNX2 i de benbildande cancercellerna, men inte i de ben-nedbrytande, som redan har höga nivåer av RUNX2. Genom att blockera RUNX2 hämmades flera centrala enzymer i steroidsyntesen särskilt då de benbildande cancercellerna odlades tillsammans med osteoklaster. Vi kunde även visa att RUNX2 på detta sätt påverkade mängden av prostata-specifikt antigen, PSA, som styrs av testosteronets bindning till sin receptor, androgenreceptorn.
I delarbete två visades alltså att RUNX2 kan driva på tumörcellernas egen förmåga att bilda testosteron och därigenom aktivera androgenreceptorn, vilket är en mycket viktig överlevnadsfunktion hos prostatacancerceller.
I det tredje delarbetet fortsatte studierna om hur RUNX2 påverkar cancercellernas tillväxt och egenskaper när de växer i skelettet, genom att cancerceller med blockerat RUNX2 injicerades i benmärgen på möss. Det är omöjligt att utifrån se hur dessa tumörer växer under försökets gång, och därför utvärderades en metod där magnetkamera användes för att följa och mäta tumörerna. Resultaten visar att magnetkamerametoden lämpar sig mycket väl för denna typ av studier och vi såg att både tumörernas storlek och benbildning mätt med magnetkamera överensstämde väl med andra analysmetoder. Med hjälp av magnetkamerametoden och andra analyser visades att tumörceller utan RUNX2 växte sämre i benmärgen och hade lägre nivåer av steroidenzymer och mindre aktivering av sin androgenreceptor jämfört med tumörceller med normal mängd RUNX2.
Sammantaget visar denna avhandling att både osteoklaster och RUNX2 påverkar centrala funktioner hos prostatacancerceller. Det finns idag många läkemedel som används för att behandla metastaserad prostatacancer och som förlänger livet på dessa patienter. Flera av dem syftar till att blockera androgenreceptorns funktion ytterligare, något som alltså tycks motverkas av både osteoklaster och RUNX2. Andra läkemedel som utprovas, som PARP-hämmare, riktar särskilt in sig på cancerceller med otillräcklig förmåga att reparera sitt DNA, en förmåga som till viss del verkar påverkas av osteoklaster. Läkemedel som hämmar osteoklasters funktion finns redan och används inom prostatacancervården, främst för att skydda skelettet och motverka så kallade skelettrelaterade händelser (SRE), men de påverkar tyvärr inte livslängden hos patienterna.
Denna avhandling visar på en möjlig positiv effekt av kombinationsbehandling av läkemedel som hämmar osteoklaster och RUNX2 med flera typer av de läkemedel som är aktuella för behandling för patienter med metastaserad prostatacancer. Detta behöver studeras vidare i djurmodeller för att sedan kunna utvärderas i kliniska studier på patienter.
Huvudhandledare: Karin Welén
Bihandledare: Jan-Erik Damber
Opponent: Docent Maria Brattsand, inst. för medicinsk biovetenskap, Umeå universitet
Betygsnämnd: Mats Geijer, Rebecka Hellsten och Dennis Larsson